Докажем это утверждение. Из первого начала термодинамики для адиабатического процесса (2.8.1) следует, что работа идеального газа равна
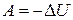 . (2.8.3)
. (2.8.3)
При адиабатическом расширении газ совершает положительную работу (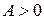 ), поэтому его внутренняя энергия уменьшается (
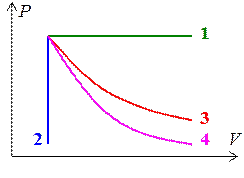
), поэтому его внутренняя энергия уменьшается (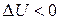 ). Это приводит к понижению температуры газа. Вследствие этого давление газа при адиабатическом расширении убывает быстрее, чем при изотермическом расширении. На рис. 2.8.1 построены, для сравнения, графики следующих процессов: 1 — изобарный, 2 – изохорный, 3 – изотермический, 4 – адиабатный.
). Это приводит к понижению температуры газа. Вследствие этого давление газа при адиабатическом расширении убывает быстрее, чем при изотермическом расширении. На рис. 2.8.1 построены, для сравнения, графики следующих процессов: 1 — изобарный, 2 – изохорный, 3 – изотермический, 4 – адиабатный.
В термодинамике выводится уравнение адиабатического процесса для идеального газа. В координатах (P, V) это уравнение имеет вид
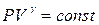 . (2.8.4)
. (2.8.4)
Это соотношение называют уравнением Пуассона. В этом уравнении безразмерная величина (показатель адиабаты)
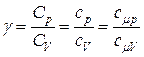 (2.8.5)
(2.8.5)
называется коэффициентом Пуассона.
Пользуясь формулами (2.7.3) — (2.7.8), получим
 , (2.8.6)
, (2.8.6)
что означает, что для одноатомного газа  , для двухатомного газа
, для двухатомного газа 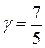 , для многоатомного газа
, для многоатомного газа 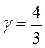 .
.
Адиабатический процесс можно отнести к изопроцессам. Теплоемкость в адиабатном процессе Cадиаб. = 0.
Работу газа в адиабатном процессе найти просто. Она равна (см. формулы (2.8.3) и (2.7.2))
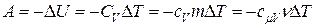 . (2.8.7)
. (2.8.7)
| | | следующая лекция ==> | |
| Адиабатический процесс | | | Железы организма |
Дата добавления: 2014-01-05 ; Просмотров: 2694 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Адиабатический процесс. Если сосуд с расширяющимся газом теплоизолировать от окружающей среды, то теплообмен будет отсутствовать, т. е. Q = 0. Процесс, происходящий при соблюдении этого условия, называется адиабатическим.
Уравнение первого начала термодинамики при учете условия Q = 0 принимает вид
0 = ΔU + A или A = – ΔU. (109)
Следовательно, при адиабатическом процессе работа совершается только за счет внутренней энергии газа. При адиабатическом расширении газ совершает работу, а его внутренняя энергия и, следовательно, температура падают. При адиабатическом сжатии работа газа отрицательна (внешняя среда производит работу над газом), внутренняя энергия и температура газа возрастают.
Адиабатический процесс можно реализовать практически и при отсутствии хорошей теплоизоляции. Но тогда необходимо вести процесс столь быстро, чтобы за время его осуществления не произошел сколько-нибудь существенный теплообмен с внешней средой.
Теплоемкость при адиабатическом процессе
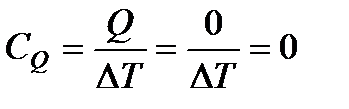 . (110)
. (110)
Выведем уравнение кривой, изображающей адиабатический процесс на рV-диаграмме. Уравнение состояния моля газа имеет вид:
При бесконечно малом изменении состояния совершаемая работа А = pdV, а изменение внутренней энергии, согласно (83), ΔU –> CVdT. Подставляя эти значения A и ΔU в уравнение первого начала термодинамики (109), получим:
Это есть уравнение адиабаты в дифференциальной форме. Поскольку оно содержит все три параметра — р, V и Т, — то для исключения одного из них воспользуемся уравнением состояния (111), предварительно продифференцировав его:
pdV + Vdp = RdT. (113)
Умножая уравнение (112) на R, а (113) — на СV искладывая их, получим
Принимая во внимание, что для идеального газа CV + R = = Ср, разделим уравнение (114) на произведение CVpV и введем обозначение
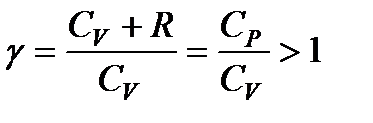 . (115)
. (115)
Тогда (114) примет вид
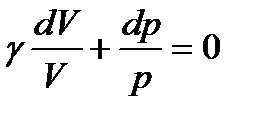 . (116)
. (116)
Учитывая, что постоянный множитель γ можно внести под знак дифференциала, преобразуем (116) к виду
Отсюда следует, что величина, стоящая в скобках, должна быть постоянной. Обозначим эту константу как ln(const). Тогда
γlnV + lnp = ln(const). (118)
Учитывая, что γlnV = lnV γ и потенцируя выражение (118), получим
Это и есть уравнение адиабаты. Его также называют уравнением Пуассона.
Поскольку γ > 1. то кривая, изображаемая этим уравнением (рис. 39), идет круче изотермы pV = const, которая для сравнения показана на том же чертеже штрих-пунктиром. Видно, что при адиабатическом расширении из точки I кривая (119) опускается ниже изотермы, т. е. газ охлаждается, а при адиабатическом сжатии кривая (119) поднимается выше изотермы, т. е. газ нагревается. Величина работы адиабатического процесса может быть особенно просто вычислена с помощью уравнения (109):
Используя формулу (115), выражение (120) можно преобразовать к виду:
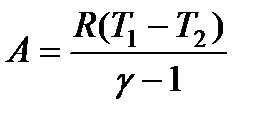 (121)
(121)
Для нахождения же конечной температуры T2 можно, комбинируя (111) и (119), получить соотношение
TV γ –1 = const. (122)
Для одноатомного газа Cv = 12,5 кДж/(кмоль*К), СP = Cv + R = 20,8 кДж/(кмоль*К), и показатель степени адиабаты равен примерно 1,67. Для двухатомных газов при обычных температурах 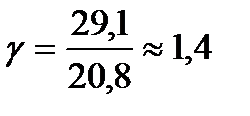 . Для многоатомных газов при возбуждении их колебательных степеней свободы теплоемкости СP и Cv имеют еще большие значения и показатель степени адиабаты
. Для многоатомных газов при возбуждении их колебательных степеней свободы теплоемкости СP и Cv имеют еще большие значения и показатель степени адиабаты
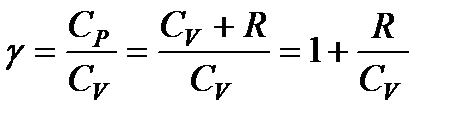 (123)
(123)
еще ближе к единице.
В быстроходных двигателях внутреннего сгорания и при истечении газов через сопла реактивных двигателей процесс расширения газа протекает настолько быстро, что его можно считать практически адиабатическим и рассчитывать по уравнению (119).
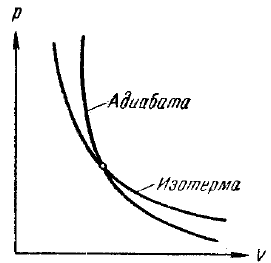
Рис. 39. Адиабата и изотерма
Так как у> 1, то из (122) следует, что при адиабатическом сжатии газ нагревается, а при адиабатическом расширении — охлаждается. Это явление находит применение в дизелях, где воспламенение горючей смеси осуществляется путем адиабатического сжатия. Нагревание газа при адиабатическом сжатии объясняется тем, что во время сжатия над газом производится работа, которая идет на увеличение его внутренней энергии. А так как внутренний энергия идеального газа зависит только от температуры, то это увеличение внутренней энергии проявляется в повышении его температуры. Аналогично объясняется и охлаждение газа при адиабатическом расширении. Охлаждение газа при адиабатическом расширении используется в холодильных машинах.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Да какие ж вы математики, если запаролиться нормально не можете. 8545 —  | 7399 —
| 7399 —  или читать все.
или читать все.
91.146.8.87 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
 Решебник по физике за 10 класс (В.А.Касьянов, 2009 год),
Решебник по физике за 10 класс (В.А.Касьянов, 2009 год),
задача №3
к главе «9. Термодинамика. §57. Адиабатный процесс. Ответы на вопросы».
3. При адиабатном сжатии газа увеличивается число упругих соударений молекул с поршнем, поэтому их кинетическая энергия и температура, возрастают.
При адиабатном расширении газа уменьшается число упругих соударений молекул с поршнем, поэтому их кинетическая энергия и температура уменьшаются.